Los valores de la constante de disociación ácida (K a) y la constante de basicidad (K b) representan la facilidad con la que un ácido o una base se disocian en iones dentro de una solución. Los ácidos fuertes y las bases fuertes se disocian por completo. Ambos tienen una K a > 1, lo cual significa que su disociación se produce hasta el final.. Como todo equilibrio posee una constante, lo mismo ocurre con la ionización de un ácido y se expresa de la siguiente manera: K = [H3O+] [A-]/ [HA] [H₂O] Termodinámicamente, se define la constante Ka en términos de actividades, no de concentraciones. Sin embargo, en disoluciones acuosas diluidas, la actividad del agua es alrededor de 1.

Como Calcular Ph BEST GAMES WALKTHROUGH
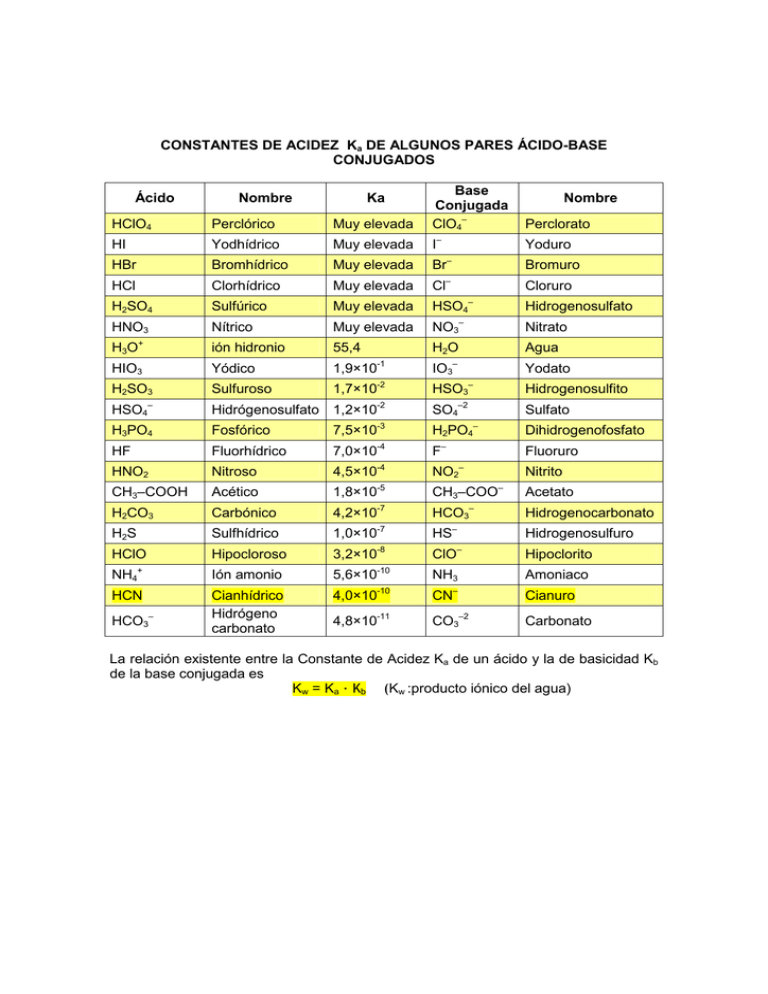
CONSTANTES DE ACIDEZ Ka DE ALGUNOS PARES ÁCIDO

27. Calcular el Valor de la Constante Ácida Ka y el Porcentaje de Ionización de un Ácido débil

Ácidos Débiles Cómo calcular Ka Constante de acidez Constante de ionización de un ácido

Constante ácida, constante básica y Kps YouTube

Constante de basicidad a partir del pH YouTube

Ejercicios pH y constante de acidez Cienciadelux

Tabla de Constante de Acidez y Basicidad PDF

Constante de Acidez y Basicidad PDF Compuestos químicos Sustancias químicas

Calcular CONSTANTE DE ACIDEZ de un ácido débil conocido el pH YouTube
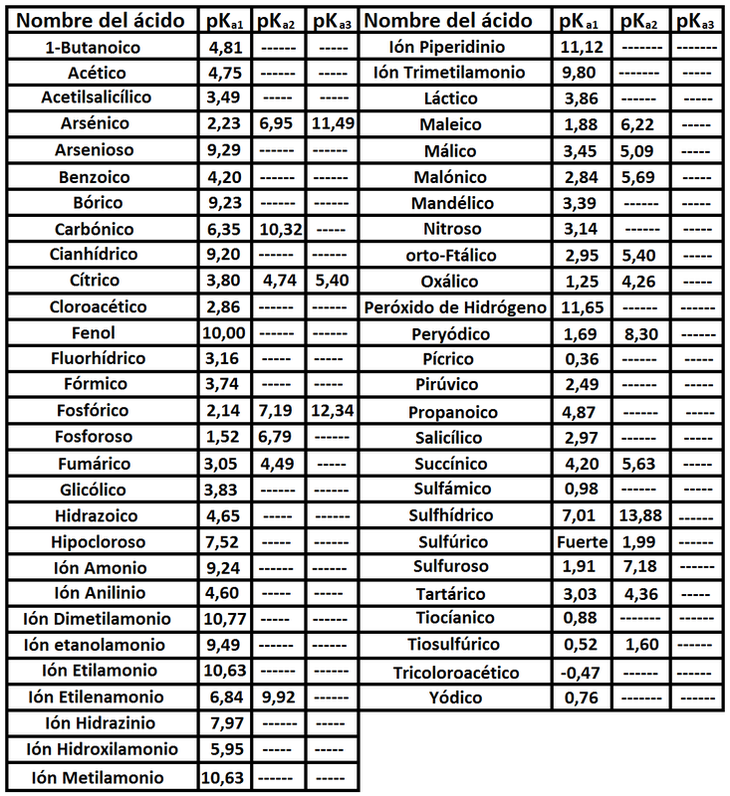
Tabla de Constantes de Acidez

La Constante de Acidez Ka constante acides ionica Química Wikisabio

Constantes de acidez y basicidad

Química General Cálculo de la Constante de disociación de un ácido Ka YouTube

pKa y pH Constante de acidez para ácidos débiles YouTube

Como calcular pH, constante de acidez cuando me dan ionización YouTube

Fuerza de los Ácidos y de las Bases Débiles y la Constante de ionización Ka y Kb YouTube

Constantes de acidez HClO y HF YouTube

pH CÁLCULO DE LA ACIDEZ DE UN MEDIO YouTube

PPT Alterações no Equilíbrio ÁcidoBase PowerPoint Presentation, free download ID900142
Resolviendo la ecuación obtenemos que x = 4,2 · 10-3 [H +] = x = 4,2 · 10-3 M. Ejercicios de Constante de Acidez Ka:. Ejercicio 1: Calcular el pH de una disolución 0,02 M de ácido débil HA con constante de acidez K a = 3,0 · 10-6. Ejercicio 2: Calcular el pK a del ácido del ejercicio anterior. Solución Ejercicio de Constante de Acidez Ka:. Una constante de disociación ácida, Ka, (también conocida como constante de acidez, o constante de ionización ácida) es la constante de equilibrio de una reacción conocida como disociación en el contexto de las reacciones ácido-base. Además, esta constante sirve como medida relativa de la fuerza de un ácido en disolución.